Сборник задач и упражнений по химии 8-9 классы к учебникам: Г. Е. Рудзитиса, Ф. Г. Фельдмана «Химия. 8 класс» и «Химия. 9 класс» - 2016 год
Амфотерные оксиды и гидроксиды - Важнейшие классы неорганических соединений - 8 класс
6.86. Как называют оксиды и гидроксиды, которые способны проявлять как основные свойства, так и кислотные? Перечислите четыре подобных оксида и соответствующих им четыре гидроксида.
6.87. Можно ли получить амфотерный гидроксид в ходе реакции соответствующего оксида с водой? Как можно получить амфотерные гидроксиды? Напишите уравнения реакций получения следующих гидроксидов:
a) Zn(OH)2 .
б) Ве(ОН)2
в) Аl(ОН)3 .
г) Сr(ОН)3
6.88. Почему при постепенном прибавлении раствора гидроксида натрия к раствору соли цинка или алюминия белый осадок гидроксида цинка вначале образуется, а затем растворяется? Как можно различить осадки амфотерных и основных нерастворимых оснований? Напишите уравнения осуществимых реакций по схемам:
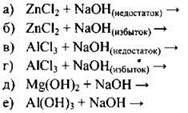
6.89. Какие свойства проявляют амфотерные оксиды и гидроксиды, реагируя с кислотами? Напишите уравнения реакций по схемам:

6.90. Какие свойства проявляют амфотерные оксиды и гидроксиды, реагируя с щелочами? Какие продукты образуются: а) в водных растворах, б) при сплавлении? Напишите уравнения реакций по схемам:
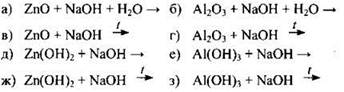
6.91. Оба оксида являются амфотерными
![]()
6.92. Оба гидроксида являются амфотерными
![]()
6.93. При взаимодействии оксида алюминия с раствором гидроксида калия образуется
![]()
6.94. При сплавлении гидроксида хрома с гидроксидом калия образуется
![]()
6.95. С помощью какого реактива можно отличить Ве(ОН)2 от Mg(OH)2?
1) NaCl .
2) Н2O
3) NaOH .
4) НСl