Сборник задач и упражнений по химии 8-9 классы к учебникам: Г. Е. Рудзитиса, Ф. Г. Фельдмана «Химия. 8 класс» и «Химия. 9 класс» - 2016 год
Железо - Металлы - 9 класс
7.266. Напишите электронную формулу атома железа. Сколько электронных уровней имеется в атоме железа? Сколько электронов имеется на внешнем уровне?
7.267. Могут ли электроны предпоследнего уровня участвовать в химических реакциях? Какие электроны являются валентными для d-металлов? Какие степени окисления характерны для железа?
7.268. Какие электроны отдает атом железа при образовании ионов Fe2+ и Fe3+? Напишите электронные формулы ионов Fe2+ и Fe3+. Какая электронная оболочка d6 или d5 более устойчива?
7.269. Для атома железа 2656Fe укажите:
а) число протонов,
б) число нейтронов,
в) число электронов,
г) массовое число.
7.270. Определите степени окисления железа а следующих соединениях:
![]()
7.271. Назовите четыре самых распространенных в земной коре элемента. Какое место занимает среди этих элементов железо?
7.272. Напишите формулы основных компонентов следующих минералов:
а) пирита, .
б) магнетита,
в) гематита, .
г) сидерита,
д) лимонита.
7.273. Определите массовую долю железа в следующих веществах:
![]()
7.274. Напишите уравнения реакций получения железа:

Укажите окислитель и восстановитель в этих реакциях.
7.275. Напишите уравнения следующих реакций:
![]()
Укажите окислитель и восстановитель в этих реакциях.
7.276. Можно ли перевозить в железных цистернах по железной дороге концентрированные растворы серной и азотной кислот? Напишите уравнения возможных реакций:

Укажите окислитель и восстановитель в этих реакциях.
7.277. Напишите уравнения возможных реакций в молекулярном и ионном виде:

Укажите окислитель и восстановитель в этих реакциях.
7.278. При восстановлении оксида железа(II) водородом было получено 3,6 г паров воды. Определите:
а) массу полученного железа,
б) объем (н.у.) израсходованного водорода.
7.279. При получении железа из оксида железа(III) методом алюминотермии получено 14 г железа. Определите:
а) массу израсходованного оксида железа(III),
б) массу израсходованного алюминия.
7.280. При электролизе водного раствора сульфата железа(II) на аноде получено 1,99 л (н.у.) газа с выходом 0,888. Определите:
а) выход железа, если его выделилось 8,4 г,
б) массу образовавшейся в растворе серной кислоты, если ее выход количественный, то есть 1,0.
7.281. Железную пластинку массой 50 г опустили в раствор, содержащий 16 г сульфата меди(II). Определите:
а) массу пластинки после окончания реакции,
б) массу образовавшегося в растворе сульфата железа(II).
7.282. Железную пластинку массой 20 г опустили в раствор соляной кислоты. Определите:
а) массу пластинки после выделения 4,48 л (н.у.) газа,
б) массу образовавшейся в растворе соли.
7.283. Железо массой 16,8 г прореагировало при нагревании с хлором. Определите:
а) массу образовавшейся соли,
б) объем (н.у.) израсходованного хлора.
7.284. При получении водорода по реакции раскаленного железа с парами воды было получено (с выходом 80%) 7,17 л (н.у.) водорода. Определите:
а) массу полученного Fe3O4, если его выход количественный, то есть 1,0,
б) массу израсходованного железа.
7.285. При обработке смеси опилок железа и алюминия избытком 10%-ного раствора соляной кислоты выделилось 8,96 л (н.у.) газа. При обработке такого же образца смеси избытком 10%-ного раствора гидроксида натрия выделилось 6,72 л (н.у.) газа. Определите массовую долю железа в исходной смеси металлов.
7.286. Число нейтронов в ядре атома железа 56Fe равно
1) 26 .
2) 30
3) 56 .
4) 82
7.287. Распределение электронов по уровням в атоме железа
1) 2, 8, 18, 2 .
2) 2, 8, 16, 2
3) 2, 8, 14, 2 .
4) 2, 8, 12, 2
7.288. Характерные степени окисления железа в соединениях
1) +2 и +3 .
2) +1 и +3
3) +2 и +4 .
4) +2 и +5
7.289. Расположите следующие оксиды в порядке уменьшения массовой доли железа в них:
а) Fe2O3,
б) FeO,
в) Fe3O4.
1) в, а, б .
2) б, а, в
3) а, в, б .
4) б, в, а
7.290. При нагревании железо реагирует с кислородом с образованием

7.291. Укажите верное суждение:
а) при взаимодействии железа с соляной кислотой образуется FeCl3;
б) при нагревании железо реагирует с хлором с образованием FeCl2.
1) верно только а
2) верно только б
3) верны оба суждения
4) оба суждения неверны
7.292. Железо реагирует с раствором
1) хлорида бари.
2) сульфата меди(II)
3) нитрата цинк.
4) сульфата магния
7.293. Укажите уравнение реакции, которая не является окислительно-восстановительной реакцией замещения
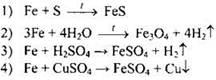
7.294. Железо можно получить в свободном состоянии
1) восстановлением его водородом из оксидов
2) электролизом водного раствора соли железа(II)
3) восстановлением его алюминием из оксидов
4) всеми перечисленными способами
7.295. Свойство, отличающее железо от многих других металлов
1) электропроводимость
2) металлический блеск
3) магнитные свойства
4) пластичность и ковкость