Поурочные разработки по химии 11 класс
Практическая работа № 3 «Решение экспериментальных задач по теме “Гидролиз. Реакции ионного обмена”» - ДИСПЕРСНЫЕ СИСТЕМЫ. РАСТВОРЫ. ПРОЦЕССЫ, ПРОИСХОДЯЩИЕ В РАСТВОРАХ - ПОУРОЧНЫЕ РАЗРАБОТКИ ПО ХИМИИ 11 класс - поурочные разработки - разработки уроков - авторские уроки - план-конспект урока - химия
Цели урока: совершенствовать навыки в выполнении химического эксперимента, соблюдая правила ОТ и ТБ; закрепить умение подтверждать теоретические знания химическим экспериментом.
Оборудование: набор реактивов на каждый стол (где имеются кислоты, щелочи, соли, индикаторы); задание практической работы на два варианта.
Ход урока
I. Организационный момент
Инструктаж учащихся по теоретической работе, ТБ и ОТ выполнения работы.
II. Выполнение работы по вариантам
|
Вариант I |
Вариант II |
|
1. Провести эксперимент между растворами электролитов. Отметить наблюдаемые явления. Дать обоснованный ответ. |
|
|
а) карбонат натрия и серная кислот. б) гидроксид натрия и сульфат цинк. |
а) хлорид бария и сульфат железа (II) б) карбонат калия и соляная кислота |
|
Уравнения реакций составить в молекулярном общем и кратком ионном виде. |
|
|
2. Исследуйте индикаторами растворы солей. |
|
|
а) сульфат цинк. б) нитрат кали. в) карбонат натри. |
а) сульфат натрия б) хлорид железа(III) в) сульфит калия |
|
Объяснить наблюдаемые явления. Составить уравнения гидролиза в молекулярном и ионном виде. |
|
|
3. Что происходит при сливании растворов электролитов? |
|
|
Хлорида алюминия и карбоната натрия. При приливании избытка АlСl3 или избытка Na2CO3 |
В раствор хлорида цинка поместили гранулу цинка. При приливании HCl или избытка ZnCl2 |
III. Домашнее задание
Подготовиться к контрольной работе № 3 по теме «Химические реакции. Дисперсные системы. Процессы, происходящие в растворах».
Ответы на задания практической работы
Вариант I

Наблюдается выделение газа и воды.
![]()
Реакция ионного обмена идет до конца, т. к. образуются газ и иода — слабый электролит.
![]()
Наблюдается выпадение осадка студенистого, белого, полупрозрачного.
![]()
Реакция ионного обмена идет до конца, т. к. образуется осадок, очень слабый электролит.
2. Результат наблюдений:
|
|
ZnSO4 |
KNO3 |
Na2CO3 |
|
Основание |
Слабое |
Сильное |
Сильное |
|
Кислота |
Сильная |
Сильная |
Слабая |
|
рн |
< 7 |
7 |
> 7 |
|
Среда |
Кислотная |
Нейтральная |
Щелочная |
|
Универсальный индикатор |
Розовый |
Зеленый |
Синий |
|
Фенолфталеин |
— |
— |
Малиновый |
|
Синий лакмус |
Красный |
Фиолетовый |
Синий |
|
Метилоранж |
Розово-красный |
Оранжевый |
Желтый |

![]() среда кислотная, гидролиз по катиону
среда кислотная, гидролиз по катиону
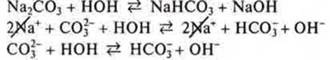
![]() среда щелочная, гидролиз по аниону
среда щелочная, гидролиз по аниону
KNO3 — гидролиза нет, т. к. соль образована сильным основанием и сильной кислотой.
3. При сливании растворов АlСl3 и Na2CO3 происходит совместный гидролиз.

Наблюдается выделение газа, если в избытке берем АlСl3; если в избытке берем Na2CO3 — то газ и осадок.
![]()
Вариант II
![]() выпадет белый осадок
выпадет белый осадок
![]()
Реакция ионного обмена идет до конца, т. к. образует осадок,
![]() наблюдается выделение газа и воды
наблюдается выделение газа и воды
![]()
Реакция ионного обмена идет до конца, т. к. образуется газ и вода.
2. Результат наблюдений:
|
|
Na2SOl |
FeCI3 |
K2SO3 |
|
Основание |
Сильное |
Слабое |
Сильное |
|
Кислота |
Сильная |
Сильная |
Слабая |
|
pH |
7 |
< 7 |
> 7 |
|
Среда |
Нейтральная |
Кислотная |
Щелочная |
|
Универсальный индикатор |
Зеленый |
Розовый |
Синий |
|
Фенолфталеин |
— |
— |
Малиновый |
|
Синий лакмус |
Фиолетовый |
Красный |
Синий |
|
Метилоранж |
Оранжевый |
Розово-красный |
Желтый |
Na2SO4 — нет гидролиза, соль образована сильным основанием и сильной кислотой.

![]() кислотная среда, гидролиз по катиону.
кислотная среда, гидролиз по катиону.

![]() среда щелочная, гидролиз по аниону.
среда щелочная, гидролиз по аниону.
![]()
При добавлении Zn, среда кислая, наблюдается выделение водорода.
![]()
При добавлении НСl, ослабляется гидролиз ZnCl2 и скорость иыделения газа уменьшается. При добавлении ZnCl2, гидролиз усиливается, скорость выделения газа возрастает.