Настольная книга учителя химии 10 класс - поурочные разработки
ГОМОЛОГИЧЕСКИЙ РЯД АЦЕТИЛЕНОВЫХ УГЛЕВОДОРОДОВ, ИЗОМЕРИЯ И НОМЕНКЛАТУРА - УГЛЕВОДОРОДЫ
Цели урока. Познакомить учащихся с гомологическим радом, изомерией и номенклатурой алкинов, с электронным и пространственным строением ацетилена. Рассмотреть способы получения ацетилена и, в первую очередь, карбидный и метановый. Раскрыть взаимосвязь органических и неорганических веществ.
Оборудование: модели молекул Стюарта — Бриглеба, плакаты «Электронное и пространственное строение ацетилена».
I. Электронное и пространственное строение ацетилена
В начале урока учитель просит ребят ответить на вопрос, как они понимают термин «непредельные углеводороды». После получения удовлетворительного ответа начинается изложение нового материала.
Оказывается, алкены — далеко не единственные представители непредельных углеводородов. Кроме двойной связи, два атома углерода могут образовывать друг с другом связь тройную. Такие соединения также являются непредельными и ненасыщенными, поскольку не до предела насыщены атомами водорода (или атомами других элементов), но в большей степени, чем алкены:

Иными словами, тройную связь можно разрушить, а освободившиеся валентности углеродных атомов насытить атомами водорода.
Простейший представитель углеводородов с тройной связью — ацетилен НС≡СН. Название этому веществу дал в 1860 г. французский химик Марселей Бертло. Именно он первым высказал предположение, что ацетилен, подобно метану и этилену, является родоначальником гомологического ряда ацетиленовых углеводородов (по международной номенклатуре алкинов).
Учитель предлагает ребятам самим вывести общую формулу соединений этого ряда. Логика рассуждения должна быть следующей.
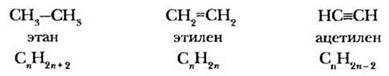
Общая формула предельных углеводородов CnH2n+2. В этиленовых углеводородах за счет отщепления двух атомов водорода образуется двойная связь, общая формула CnH2n. В алкинах появляется еще одна связь между атомами углерода. Следовательно, они содержат еще на два атома водорода меньше, общая формула CnH2n-2.
Учитель вновь возвращается к повторению сведений о гибридизации атома углерода. Учащиеся вспоминают, что в алканах все атомы углеродного скелета находятся в состоянии sp3-гибридизации. В алкенах атомы углерода, связанные двойной связью, имеют sp2-гибридизацию. Какой тип гибридизации встречается в молекуле ацетилена? Учитель с помощью учеников выясняет, что в состоянии sp-гибридизации атом углерода имеет четыре орбитали: две sp-гибридные и две негибридизованные p-орбитали. За счет первых двух углерод образует σ-связи, за счет двух вторых — π-связи (рис. 12).

Рис. 12. σ- и π-связи в молекуле ацетилена
Комментируя рисунок, учитель попутно задает вопрос на повторение и закрепление материала: какие связи относятся к σ- и π-типу?
Тип гибридизации определяет пространственное расположение атомов в молекуле. Центры ядер всех четырех атомов в ацетилене расположены на одной прямой, т. е. молекула линейна, величина угла ∠HCC составляет 180°.
Учащимся несложно самим дать ответы на два следующих вопроса:
1. Какая связь короче: двойная или тройная? Для иллюстрации правильного ответа учитель приводит числовые данные: длина тройной С≡С связи 0,120 нм, а длина двойной и одинарной — соответственно, 0,133 и 0,154 нм.
2. Возможна ли для ацетиленовых углеводородов геометрическая изомерия? Если ребята затрудняются дать ответ, учитель для большей наглядности изображает на доске полные структурные формулы ацетилена и этилена.

II. Гомологический ряд алкинов. Изомерия и номенклатура
С помощью моделей молекул или на доске учитель изображает «гомологические превращения» одного ацетиленового углеводорода в его гомолог: заменой атома водорода на метальный радикал этин превращается в пропин. А вот бутинов может существовать уже два. Это изомеры, различающиеся положением кратной связи. Начиная с пентина, у алкинов появляется изомерия углеродного скелета. Учитель может подписать под формулой каждого изображенного на доске алкина его название, продиктованное классом. Поскольку никаких особенностей в номенклатуре алкинов нет, остается лишь обратить внимание на замену суффикса -ан на -ин в названии ацетиленовых углеводородов, да на то, что этин чаще называют ацетиленом, а пропин — метилацетиленом.

Можно отметить, что число изомерных алкинов меньше, чем для алкенов с тем же числом углеродных атомов. С чем это связано? Конечно, с отсутствием цис-траис-изомерии.
III. Способы получения алкино.
1. Пиролиз метана (метановый метод). В 1868 г. М. Бертло, пропуская через метан электрический разряд, обнаружил в смеси образующихся газов ацетилен. Это было неожиданно для самого учёного. Учитель просит ребят вспомнить, что происходит с метаном при нагревании его без доступа воздуха? (Пиролиз.) Метан при разложении образует два простых вещества — углерод (сажа) и водород. Оказывается, этот процесс происходит через образование ряда промежуточных продуктов, из которых важнейший — ацетилен. Как же остановить реакцию на стадии получения этина, предотвратив его дальнейшее разложение на С и Н2? Ответ подсказал опыт Бертло. Воздействие температуры должно быть очень кратковременным, то есть метан попадает в нагретую зону реактора на доли секунды, после чего продукты реакции резко охлаждаются. Пиролиз метана используется для промышленного синтеза ацетилена с 1936 г.
Для непрофильных классов приведенной выше информации и уравнения реакции вполне достаточно. Учащимся профильных классов можно несколько расширить представления о данном способе % получения метана.
Во-первых, в данную реакцию вступает не только метан, но и его ближайшие гомологи (этан, пропан), а также бензиновая и керосиновая фракции нефти. Первое обстоятельство позволяет использовать в качестве сырья для получения ацетилена природный газ. Во втором случае происходит последовательный крекинг алканов с образованием все более коротких «кусочков», превращающихся в конечном счете в молекулу ацетилена.
Модификацией метанового способа получения ацетилена является термоокислительный пиролиз природного газа. При недостатке кислорода образуется ещё один побочный продукт реакции — оксид углерода (II):
![]()
Экономически этот процесс оправдывается использованием побочных продуктов (СО и Н2) для синтеза спиртов, а также сжиганием части водорода для поддержания высокой температуры процесса.
2. Дегидрогалогенирование дигалогеналканов. Один из способов получения соединений с двойной связью — отщепление молекулы галогеноводорода от галогеналкана. Учащиеся вспоминают эту реакцию, и учитель под их диктовку записывает ее на доске. Затем ставит проблему: можно ли подобным образом «построить» тройную связь? Что для этого необходимо? Вероятно, для этого нужно взять производное предельного углеводорода с двумя атомами галогена. Как должны быть расположены эти два атома в углеродной цепи? Теоретически существует два возможных варианта: два атома галогена при одном либо при соседних углеродных атомах. Действительно, в 60-х гг. XIX в. молодым русским ученым М. Мясникову и В. И. Савичу удалось получить ацетилен взаимодействием 1,2-дибромэтана с кипящим спиртовым раствором гидроксида калия:

Эти превращения демонстрируют генетическую связь между соединениями предельного, этиленового и ацетиленового рядов.
Указанный способ получения алкинов имеет скорее теоретическое, чем практическое значение. Отщепление второй молекулы галогеноводорода в большинстве случаев требует более сильного основания, чем гидроксид калия (например, раствор металлического натрия в жидком аммиаке). Это обстоятельство не позволяет использовать метод в промышленном масштабе.
3. Карбидный способ. Впервые получил ацетилен и изучил некоторые его химические свойства английский химик Э. Дэви. В 1836 г. при действии воды на карбид кальция он получил бесцветный газ, горящий красноватым коптящим пламенем. Ученый попытался определить его состав и высказал предположение, что полученный им «светильный газ» можно использовать для освещения.
Учитель обращает внимание на то, что карбиды различных металлов при гидролизе ведут себя по-разному. В одних случаях в качестве органического продукта выделяется метан, в других — ацетилен. Но знать необходимо только две реакции: карбида алюминия и карбида кальция с водой:
![]()
Учащиеся профильных классов должны уметь писать реакции карбидов не только с водой, но и с растворами кислот:
![]()
Обязательно нужно напомнить, что карбид кальция получают в промышленности взаимодействием углерода (кокс) с оксидом кальция, который образуется при прокаливании известняка СаСО3:

Благодаря доступности сырья, карбидный метод получения ацетилена также используется в промышленности.
Наряду с традиционными заданиями и упражнениями на изомерию, номенклатуру, способы получения алкинов, на данном уроке можно вспомнить задачи на массовую долю примеси.
Задание 1
1-й уровень
Среди приведенных углеводородов выберите формулы алкинов и составьте структурные формулы всех возможных изомеров: С3Н6, С4Н6, С2Н2, С6Н14, С6Н6, С5Н8.
2-й уровень
Составьте структурные формулы всех изомерных гексинов и назовите каждый углеводород по международной номенклатуре.
Задание 2
1-й уровень
Напишите не менее трех реакций, с помощью которых можно получить ацетилен.
2-й уровень
Какие из указанных галогенпроизводных пригодны для получения алкинов: 2,2-дибромпентан; 1,3-дихлорбутан; 1,1-дибром-3-метилбутан; 2,3-дибром-3-метилпентан; 3,4-дихлоргексан. Напишите уравнения соответствующих реакций. Назовите полученные алкины.
Задание 3
1-й уровень
Из 40 г технического карбида кальция был получен ацетилен, который при нормальных условиях занимал объем 11,2 л. Рассчитайте массовую долю примесей в образце карбида кальция.
2-й уровень
Какую массу природного известняка, содержащего 90% карбоната кальция, необходимо взять для получения 1 т карбида кальция?